Surfactanții, acele mici molecule mici care au tot felul de proprietăți cool, pot avea unele interacțiuni cu adevărat interesante cu proteinele. În calitate de furnizor de surfactanți, am văzut de prima dată cum aceste două substanțe o pot amesteca în diferite moduri și sunt lucruri destul de fascinante. Deci, să ne aruncăm în modul în care surfactanții interacționează cu proteinele.
Bazele tensioactivilor și proteinelor
În primul rând, să trecem repede peste ce sunt surfactanții și proteinele. Surfactanții sunt compuși care scad tensiunea de suprafață între două lichide sau între un lichid și un solid. Au un cap hidrofil (apă - iubitor) și o coadă hidrofobă (apă - ură). Această structură unică le permite să facă tot felul de lucruri, cum ar fi micelele în soluție.
Pe de altă parte, proteinele sunt molecule mari, complexe, formate din aminoacizi. Acestea joacă roluri cruciale în corpul nostru, cum ar fi catalizarea reacțiilor chimice, transportul moleculelor și oferind sprijin structural. Proteinele au o structură specifică cu trei dimensiuni, care este super importantă pentru funcția lor. Temniță cu acea structură și poți încurca cu ceea ce face proteina.

Interacțiuni fizice
Unul dintre principalele moduri în care surfactanții interacționează cu proteinele este prin mijloace fizice. Cozile hidrofobe ale surfactanților pot interacționa cu regiunile hidrofobe ale proteinelor. Proteinele au adesea aminoacizi hidrofobi îngropați în structura lor pentru a le menține stabile într -un mediu apos. Când surfactanții vin, cozile lor hidrofobe se pot introduce în aceste buzunare hidrofobe ale proteinei.
Această interacțiune poate schimba structura proteinei. De exemplu, ar putea determina să se desfășoare proteina sau să se denatureze. Atunci când o proteină se denorează, își pierde forma normală cu trei dimensiuni și, ca urmare, funcția sa poate fi afectată. Gândiți -vă la el ca și cum ar fi să vă desparti de un puzzle construit cu atenție. Odată ce este în bucăți, nu poate face ceea ce trebuia să facă.
Dar nu este o veste proastă. În unele cazuri, surfactanții pot ajuta de fapt proteinele să rămână stabile. De exemplu, în unele procese industriale în care proteinele trebuie să fie păstrate în soluție, surfactanții pot preveni agregarea proteinelor. Agregarea este atunci când proteinele se reunesc, ceea ce poate duce și la pierderea funcției. Surfactanții pot acoperi proteinele, creând un fel de strat de protecție care le menține separate unul de celălalt.
Interacțiuni chimice
Surfactanții pot avea, de asemenea, interacțiuni chimice cu proteine. Unii tensioactivi au grupuri încărcate în capetele lor hidrofile. Aceste grupuri încărcate pot interacționa cu aminoacizii încărcați pe suprafața proteinelor. De exemplu, un agent tensioactiv încărcat pozitiv ar putea interacționa cu un aminoacid încărcat negativ pe proteină.
Aceste interacțiuni electrostatice pot afecta solubilitatea și stabilitatea proteinei. Dacă un agent tensioactiv se leagă de o proteină prin forțe electrostatice, acesta poate modifica sarcina generală a complexului proteic - agent tensioactiv. Această schimbare în sarcină poate face complexul mai mult sau mai puțin solubil în apă, în funcție de circumstanțe.
Aplicații în diferite industrii
Interacțiunea dintre surfactanți și proteine are o gamă largă de aplicații în diferite industrii. În industria farmaceutică, surfactanții sunt folosiți pentru a îmbunătăți solubilitatea și stabilitatea medicamentelor pe bază de proteine. De exemplu, unii anticorpi monoclonali, care sunt proteine utilizate în medicină, pot fi formulați cu surfactanți pentru a preveni agregarea în timpul depozitării și livrării.
În industria alimentară, surfactanții sunt folosiți pentru emulsionarea proteinelor din produse precum maioneză și pansamente de salată. Ele ajută la ferirea fazelor de ulei și apă de separare, ceea ce este important pentru textura și raftul - viața acestor produse.

În industria cosmetică, surfactanții sunt folosiți în șampoane și balsamuri pentru a interacționa cu proteinele din păr. Acestea pot ajuta la curățarea părului prin îndepărtarea murdăriei și a uleiului și, în același timp, pot condiționa părul interacționând cu proteinele din arborele părului pentru a -l face mai neted și mai strălucitor.
Surfactanți specifici și interacțiunile lor
Să vorbim despre unii surfactanți specifici pe care îi furnizăm. LuaTrifluorometanesulfinat de sodiu nr.: 2926 - 29 - 6. Acest agent tensioactiv are unele proprietăți unice datorită prezenței grupului trifluometil. Atomii de fluor din grup fac ca agentul tensioactiv să fie mai hidrofob în comparație cu surfactanții care nu fluorurați.
Când vine vorba de interacțiunea cu proteinele, hidrofobicitatea crescută a trifluorometanesulfinatului de sodiu înseamnă că poate avea interacțiuni mai puternice cu regiunile hidrofobe ale proteinelor. Acest lucru ar putea duce la schimbări mai semnificative în structura proteinei, dar înseamnă, de asemenea, că ar putea fi mai eficient la prevenirea agregării proteice în unele cazuri.
Un alt agent tensioactiv pe care îl oferim esteFluorură trifluorometanesulfonil ≥98,0%. Acest compus poate reacționa cu anumiți aminoacizi în proteine în condiții specifice. De exemplu, poate reacționa cu aminoacizi care au grupuri nucleofile, cum ar fi cisteina și serina. Această reacție poate modifica structura și funcția proteinei, ceea ce poate fi util în unele aplicații de cercetare în care doriți să studiați rolul aminoacizilor specifici într -o proteină.
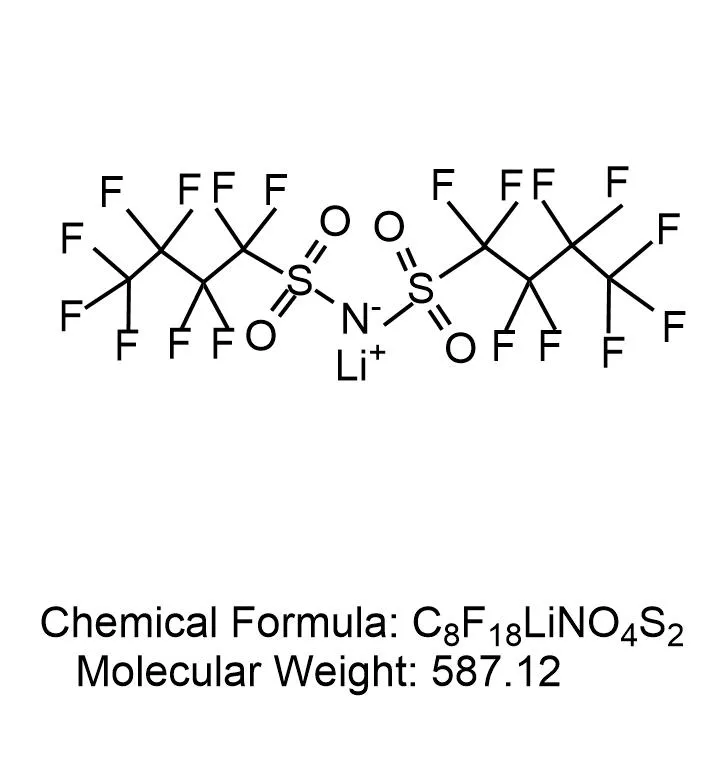
≥99,0% litiu bis (1,1,2,2,3,3,4,4,4 - nonafluoro - 1 - butanesulfonil) imideeste un agent tensioactiv cu o structură relativ mare și complexă. Are mai multe grupuri fluorurate, care îi conferă proprietăți unice de suprafață - active. Când interacționați cu proteinele, poate forma agregate complexe cu proteine datorită dimensiunii și hidrofobicității sale. Aceste agregate pot avea proprietăți diferite în comparație cu proteina sau agentul tensioactiv individual și ar putea fi utile în aplicații precum administrarea de medicamente.
Factori care afectează interacțiunea
Există mai mulți factori care pot afecta modul în care surfactanții interacționează cu proteinele. Unul dintre cei mai importanți factori este concentrația agentului tensioactiv. La concentrații scăzute, surfactanții s -ar putea lega doar de suprafața proteinei într -un mod reversibil. Dar pe măsură ce concentrația crește, mai mulți surfactanți se pot lega de proteină, ceea ce duce la modificări structurale mai semnificative.
PH -ul soluției joacă, de asemenea, un rol. Proteinele au sarcini diferite la valori de pH diferite, iar surfactanții cu grupuri încărcate vor interacționa diferit cu proteina în funcție de pH. De exemplu, la un pH scăzut, o proteină ar putea avea o încărcare pozitivă netă, iar un agent tensioactiv încărcat negativ se va lega mai puternic de acesta.
Temperatura este un alt factor. Temperaturile mai ridicate pot crește energia cinetică a moleculelor, ceea ce poate afecta legarea surfactanților la proteine. În unele cazuri, temperaturile mai ridicate pot determina proteina să se denatureze mai ușor în prezența agenților tensioactivi.
Concluzie
Interacțiunea dintre surfactanți și proteine este o zonă de studiu complexă și fascinantă. În calitate de furnizor de surfactanți, învățăm în mod constant mai multe despre cum funcționează aceste interacțiuni și cum le putem folosi în avantajul nostru în diferite industrii. Indiferent dacă îmbunătățește stabilitatea medicamentelor pe bază de proteine sau îmbunătățește textura produselor alimentare, surfactanții au multe de oferit.
Dacă sunteți interesat să aflați mai multe despre surfactanții noștri și despre cum pot interacționa cu proteinele din aplicația dvs. specifică, ne -ar plăcea să discutăm. Contactați -ne pentru a începe o discuție de achiziții și să vedem cum putem lucra împreună pentru a face proiectele dvs. un succes.
Referințe
- Tanford, C. (1973). Efectul hidrofob și organizarea materiei vii. Science, 181 (4096), 261 - 268.
- Creighton, Te (1993). Proteine: structuri și proprietăți moleculare. Wh Freeman and Company.
- Israelachvili, JN (2011). Forțe intermoleculare și de suprafață. Presă academică.
